2023年4月14日,上海科技大学生命学院特聘教授周斌研究员在学术期刊《自然遗传学》(Nature Genetics)上发表了研究论文“Dual genetic tracing reveals a unique fibroblast subpopulation modulating cardiac fibrosis”。研究发现,心内膜起源的成纤维细胞(Endocardium-derived fibroblast, EndoFb)是调节心脏纤维化的独特成纤维细胞亚群。

图1. 论文截图
心力衰竭每年都会导致全球范围内大量的个体致病或死亡。在心脏损伤早期,心脏成纤维细胞被激活并分化成具有收缩性的肌成纤维细胞,产生大量的胞外基质,维持心脏基本功能。然而,成纤维细胞增殖过多会导致胞外基质的过度积累并导致心脏弹性减弱,最终促使心力衰竭。因此,了解驱动心脏纤维化病理过程的基本机制,为开发治疗心脏纤维化的潜在靶标提供新的思路和见解,对缓解心脏衰竭、提高患者生存质量具有临床指导意义。
之前研究心脏成纤维细胞亚群主要用单同源重组酶介导的谱系示踪方法,其标记的不特异性使得研究人员无法对成纤维细胞在稳态和损伤情况下的表型探究,也无法仅对成纤维细胞进行特异性的遗传操作,这就使得探究不同成纤维细胞亚群对心脏纤维化和心力衰竭影响的潜在机制成为一个难题。
本研究中,研究人员首先构建了EndoFb-tracer系统,发现在心脏发育和成体稳态情况下EndoFb具有非常明显的区域性分布特征,在心脏压力负荷下(TAC模型),EndoFb比其他成纤维细胞亚群更具增殖潜能。通过Fb-ProTracer系统,研究人员无偏好地评估成纤维细胞在稳态或损伤后的增殖情况,揭示了TAC后成纤维细胞的增殖区域性。利用EndoFb-DTR系统,研究人员在遗传学水平上特异性清除EndoFb,证实了EndoFb调控心脏纤维化和病理性心肌重塑。通过构建成纤维细胞亚群特异性基因敲除Ctnnb1-KO系统,揭示Wnt信号通路是TAC后调控EndoFb扩张的重要分子机制。
以上研究揭示了EndoFb在心脏纤维化病理过程中具有重要的调节功能,为未来心脏疾病的治疗提供了一个新的潜在靶点。该研究也展示了使用双重组酶介导的遗传谱系示踪技术对于研究体内某个细胞亚群在特定疾病发展过程中的机制和功能的优势,为研究亚群细胞对多种疾病的发生发展提供新的思路。
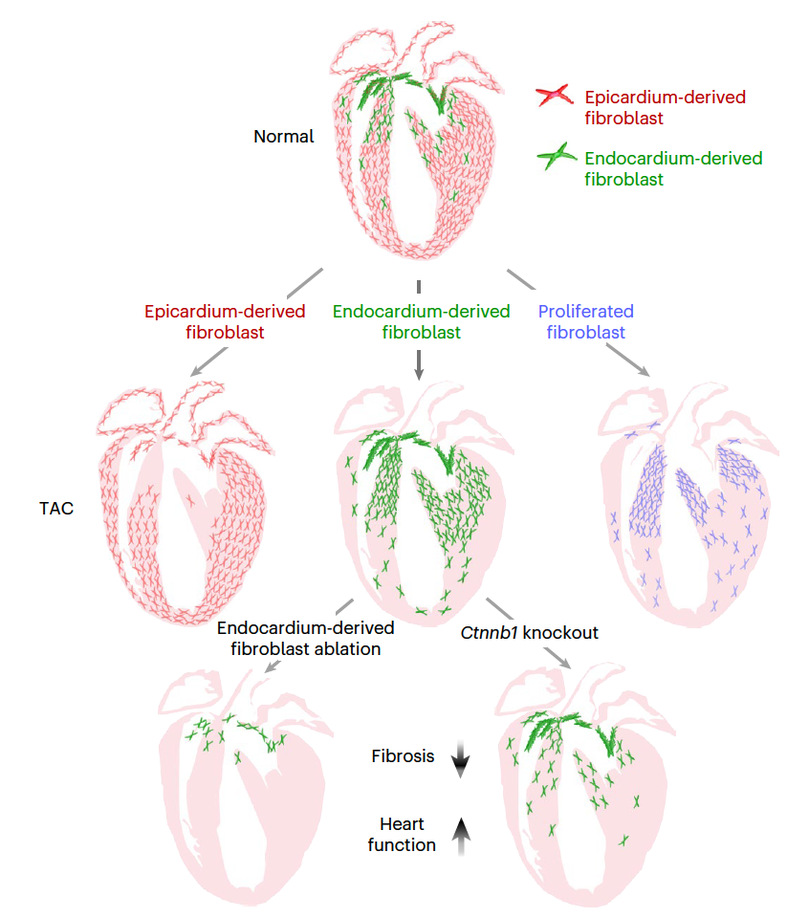
图2. 靶向EndoFb可减缓心脏纤维化和心功能衰竭示意
上海科技大学2019级博士生韩茂莹、分子细胞卓越创新中心2021级博士生刘子鑫和上海科技大学2022级博士生刘磊为共同一作,生命学院特聘教授周斌研究员为通讯作者。
文章链接:https://doi.org/10.1038/s41588-023-01337-7